Структурную основу всех тканей живых организмов составляют белки, поэтому гипертрофия любой ткани, в том числе и мышечной, тесно связана с интенсивностью синтеза и катаболизма белка в данной ткани. Достоверно установлено, что регулярная тренировка вызывает гипертрофию скелетных мышц, сопровождающуюся увеличением массы сухого остатка мышц (Н.Н.Яковлев и др. 1957). Под воздействием тренировки в мышцах увеличивается содержание сократительных белков — миозина и актина, саркоплазматических и митохондриальных белков, а также мышечных ферментов (Н.Н.Яковлев 1974).
Установлено, что физическая нагрузка угнетает синтез белка в мышечной ткани непосредственно во время упражнения и активизирует катаболизм белка в начальный восстановительный период (Н.Н.Яковлев 1974), (А.А.Виру, Н.Н.Яковлев 1988). Следовательно, функциональная гипертрофия мышц происходит именно за счёт активизации синтеза белка, но никак не в результате снижения интенсивности распада белка при сохранении прежнего уровня интенсивности синтеза белка.
Тем не менее, сами механизмы воздействия тренировки на интенсивность синтеза белка в мышцах до настоящего времени в достаточно полной мере ещё не изучены.
Регуляция синтеза белка на уровне транскрипции мРНК
Интенсивность синтеза белка может зависеть от множества факторов и регулироваться на всех этапах его биосинтеза. Однако ключевым этапом регуляции белкового синтеза считается этап транскрипции мРНК — первый этап биосинтеза белка, в ходе которого происходит считывание с ДНК ядра клетки информации о последовательности аминокислот в белковой молекуле и запись этой информации в молекуле матричной РНК, на основе которой затем в цитоплазме клетки осуществляется сборка белковой молекулы.
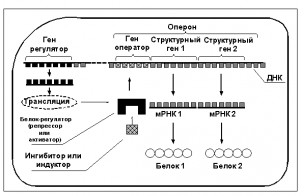
Согласно общепринятой на сегодня концепции Ф.Жакоба и Ж.Моно (излагается по Т.Т.Берёзов и Б.Ф.Коровкин 1998, М.Сингер и П.Берг 1998), в молекуле ДНК имеются не только структурные гены (то есть те гены, которые кодируют белки, обеспечивающие функционирование клетки), но также и гены, регулирующие активность самих структурных генов — то есть так называемые “гены-операторы” и “гены-регуляторы” (см. рис. 1).
Комплекс генов, состоящий из гена-оператора и одного или нескольких структурных генов, экспрессия (то есть процесс активизации транскрипции мРНК на данном гене и синтез готовой мРНК) которых регулируется совместно, называется опероном. Транскрипция мРНК на структурных генах оперона возможна лишь тогда, когда ген-оператор находится в активном состоянии. На ген-оператор могут воздействовать специфические белки, экспрессируемые геном-регулятором, которые могут как блокировать ген-оператор (в этом случае регуляторный белок называется репрессором, а схема регуляции называется отрицательной регуляцией), так и активировать ген-оператор (в этом случае регуляторный белок называется активатором транскрипции, а схема регуляции называется положительной регуляцией).
В свою очередь, регуляторные белки подвержены влиянию определённых низкомолекулярных веществ, которые при соединении с регуляторным белком изменяют его структуру так, что тот либо получает возможность связаться с геном-оператором, либо возможность связывания белка-регулятора с геном-оператором блокируется. Набор регуляторных белков, а также низкомолекулярных веществ, индуцирующих или ингибирующих транскрипцию мРНК, индивидуален для каждого оперона и до настоящего времени для большинства генов человека в точности не определён.
Наиболее полно изучена регуляция транскрипции ферментов в клетках прокариот, то есть простейших безъядерных одноклеточных живых существ. Как правило, индукторами транскрипции мРНК того или иного фермента у прокариот выступают субстраты — исходные вещества, подвергающиеся в клетке определённым превращениям под действием фермента. А продукты протекающих в клетке химических реакций, являющиеся результатом переработки субстратов, могут выполнять роль ингибиторов транскрипции мРНК фермента. Таким образом, при появлении в клетке субстратов, требующих дальнейшей переработки, индуцируется синтез ферментов, осуществляющих такую переработку, а при снижении концентрации субстратов и накоплении продуктов реакции транскрипция фермента блокируется.
Например, если бактерии E.coli попадают в раствор глюкозы, то они приспосабливаются к перевариванию именно глюкозы, то есть ферменты, расщепляющие более сложные углеводы, у этих бактерий не вырабатываются. Если же глюкозу в питательном растворе заменить молочным сахаром — лактозой, то E.coli некоторое время не могут питаться и размножаться, поскольку ген лактазы — фермента, расщепляющего лактозу на глюкозу и галактозу, блокирован у данных бактерий белком-репрессором, и они не синтезируют данный фермент. Однако уже через некоторое время после замены питательной среды лактоза, поглощаемая бактериями E.coli, соединяется с белком-репрессором гена, кодирующего лактазу, и репрессор теряет способность связываться с ДНК и перестает блокировать синтез мРНК лактазы. В результате таких процессов в бактериальной клетке активируется синтез нужного фермента, бактерии получают возможность переваривать молочный сахар, и снова начинают размножаться. При этом белок-репрессор продолжает постоянно вырабатываться бактериальной клеткой, но новые молекулы лактозы связываются с репрессором и инактивируют его. Как только бактерии переработают всю лактозу, инактивирование белка-респрессора лактозой становится невозможным и активный репрессор вновь блокирует ген, кодирующий лактазу — фермент, потребность в котором уже отпала. Таков механизм, благодаря которому через активность генов регулируется адаптивная реакция клетки на изменение условий её существования.
Регуляция транскрипции в клетках эукариот, то есть живых существ, клетки которых имеют ядра, может происходить по принципиально схожим, но гораздо более сложным схемам, так как процессы транскрипции мРНК и сборки на её основе белковой молекулы разобщены как мембраной ядра, так и временным интервалом (у эукариот синтез мРНК происходит в ядре клетки, а сборка белковой молекулы осуществляется вне ядра, непосредственно в цитоплазме). В многоклеточных организмах преобладает положительная регуляция активности генов, и для каждого оперона имеется не менее пяти участков ДНК, с которыми должно произойти связывание специфических белков-регуляторов для того, чтобы началась транскрипция структурных генов данного оперона. Для ряда оперонов в качестве индукторов транскрипции мРНК могут выступать стероидные гормоны.